
Orbital s có dạng hình tròn, hình số tám nổi, hình cầu, hình bầu dục
Với giải Câu 2 trang 22 Hóa học lớp 10 Kết nối tri thức với cuộc sống chi tiết trong Bài 3: Cấu trúc lớp vỏ electron nguyên tử giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 10 Bài 3: Cấu trúc lớp vỏ electron nguyên tử
Câu 2 trang 22 Hóa học 10: Orbital s có dạng
A. hình tròn
B. hình số tám nổi
C. hình cầu
D. hình bầu dục
Phương pháp giải:
Các orbital s có dạng hình cầu và orbital p có dạng hình số 8 nổi
Lời giải:
Các orbital s có dạng hình cầu
Đáp án C
Lý thuyết Chuyển động của electron trong nguyên tử
Đầu thế kỉ XX, người ta vẫn cho rằng các electron chuyển động xung quanh hạt nhân nguyên tử theo những quỹ đạo tròn hay bầu dục, giống như quỹ đạo của các hành tinh quay xung quanh Mặt Trời.
![]()
Theo mô hình hiện đại, trong nguyên tử, electron chuyển động rất nhanh, không theo quỹ đạo xác định. Vùng không gian xung quanh hạt nhân có xác suất tìm thấy electron là lớn nhất (khoảng 90%) và có thể hình dung vùng không gian đó như một đám mây electron, được gọi là orbital nguyên tử (kí hiệu là AO).
1. Hình dạng orbital nguyên tử
Dựa trên sự khác nhau về hình dạng, sự định hướng của orbital trong nguyên tử để phân loại orbital thành orbital s, orbital p, orbital d và orbital f. Các orbital s có dạng hình cầu và orbital p có dạng hình số 8 nổi.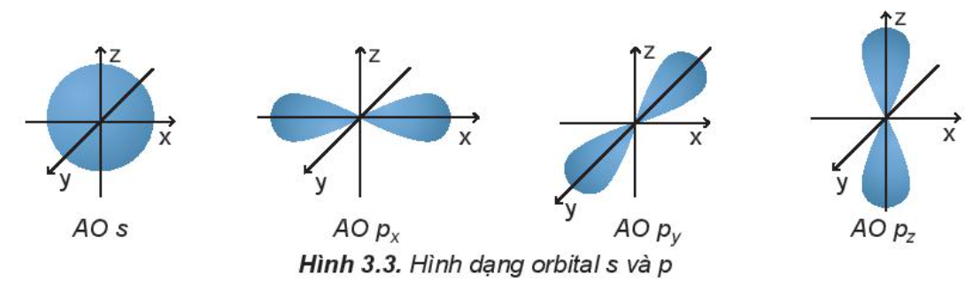
2. Ô orbital
Một AO được biểu diễn bằng một ô vuông, gọi là ô orbital .
Trong 1 orbital chỉ chứa tối đa 2 electron có chiều tự quay ngược nhau. Nếu orbital có 1 electron thì biểu diễn bằng một mũi tên đi lên (↑), nếu orbital có 2 electron thì được biểu diễn bằng 2 mũi tên ngược chiều nhau, mũi tên đi lên viết trước (↑↓).
Xem thêm các bài giải Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Mở đầu trang 21 Hóa học 10:Trong nguyên tử các electron chuyển động như thế nào? Sự sắp xếp các electron ở các lớp, các phân lớp tuân theo nguyên lí và quy tắc nào?...
Câu 1 trang 22 Hóa học 10: Mô hình hiện đại mô tả sự chuyển động của electron trong nguyên tử như thế nào?...
Câu 3 trang 22 Hóa học 10: Quan sát Hình 3.3 và nêu sự định hướng của các AO p trong không gian...
Câu 4 trang 23 Hóa học 10: Hãy cho biết tổng số electron tối đa chứa trong...
Câu 5 trang 23 Hóa học 10: Lớp electron có số electron tối đa gọi là lớp electron bão hòa. Tổng số electron tối đa có trong các lớp L và M là...
Câu 6 trang 24 Hóa học 10: Cấu hình electron của nguyên tử có Z = 16 là...
Câu 7 trang 24 Hóa học 10: Biểu diễn cấu hình electron của các nguyên tử có Z = 8 và Z = 11 theo ô orbital...
Câu 8 trang 25 Hóa học 10: Silicon được sử dụng trong nhiều ngành công nghiệp: gốm, men sứ, thủy tinh, luyện thép, vật liệu bán dẫn,… Hãy biểu diễn cấu hình electron của nguyên tử silicon (Z = 14) theo ô orbital, chỉ rõ việc áp dụng các nguyên lí vững bền, nguyên lí Pauli và quy tắc Hund...
Câu 9 trang 25 Hóa học 10: Chlorine (Z = 17) thường được sử dụng để khử trùng nước máy trong sinh hoạt. Viết cấu hình electron của nguyên tử chlorine và cho biết tại sao chlorine là phi kim...
Câu 10 trang 25 Hóa học 10: Nguyên tố calcium giúp cho xương chắc, khỏe. Cấu hình electron lớp ngoài cùng của nguyên tử calcium là 4s2. Hãy viết cấu hình electron đầy đủ của nguyên tử calcium và cho biết nguyên tố calcium là kim loại, phi kim hay khí hiếm...
Xem thêm các bài giải SGK Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 2: Nguyên tố hóa học
Bài 3: Cấu trúc lớp vỏ electron nguyên tử
Bài 4: Ôn tập chương 1
Bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một chu kì và trong một nhóm
Link nội dung: https://thietkethicongnoithat.edu.vn/orbital-s-a53645.html